
Se proprio non avete niente da fare e avete i mezzi, un esperimento interessante può essere la sintesi di rubini a partire dall’alluminio.
Per dovere di cronaca, ricordiamo che i rubini sono dei corindoni con impurità di cromo nel reticolo intorno 1%. Il corindone infatti è un minerale fortemente allocromatico e la presenza di altri ioni metallici gli conferisce diverse colorazioni.
Per prima cosa dobbiamo reperire i reagenti. Volendo partire da alluminio abbiamo una discreta scelta di oggetti da sacrificare nel nostro esperimento, ma quale utilizzare? L’idea di base è che più è puro meglio è, quindi il buon vecchio rotolo di carta stagnola da cucina fa al caso nostro in quanto è alluminio di grado alimentare.

carta di alluminio
Sempre al supermercato possiamo trovare alcune delle altre materie prime quali acqua demineralizzata e idrossido di sodio (comunemente chiamato soda caustica – in alternativa a questo reagente potete usare del carbonato di sodio).

soda caustica
Cosa che non è detto che ci sia al supermercato ma che sicuramente troverete in ferramenta è l’acido cloridrico concentrato (una soluzione intorno al 30% va benissimo) che spesso viene venduto sotto il nome di “acido muriatico”. Infine servirà dell’ossido cromico (la nostra impurità che impartirà il colore al rubino) che è possibile trovare in colorificio in quanto usato come verde-cromo.

verde cromo
Iniziamo ora la trasformazione dell’alluminio secondo la reazione:
Al + 3 HCl -> AlCl3 + 1,5 H2
Eh già, questa reazione, oltre al cloruro di alluminio che ci serve, sviluppa idrogeno che è infiammabile quindi conviene stare in un posto bene ventilato e lontano da eventuali inneschi. Inoltre la reazione è esotermica, quindi non solo evaporerà dell’idrogeno bello caldo ma tra i vapori che si solleveranno ci sarà anche un po’ di acido cloridrico, quindi magari evitate di sniffare quello che esce e attenti agli eventuali schizzi di acido. Una volta prese le necessarie precauzioni (tra cui occhiali di protezione e guanti) si prende un foglio di alluminio, lo si pesa e lo si spezzetta; in un contenitore di vetro (anche un comune barattolo va bene purchè sia pulito e di un volume almeno doppio rispetto a quello dell’acido) si versa una quantità di acido cloridrico che sia in eccesso rispetto alla stechiometria di reazione (un 20% in più va bene – va comunque annotata la quantità utilizzata perché poi andrà neutralizzato).
Una volta che tutto il metallo è stato dissolto, si attende che la soluzione si raffreddi possibilmente fino a temperatura ambiente in quanto la prossima reazione sarà sempre molto esotermica.
Il prossimo passaggio sarà la formazione di idrossido di alluminio secondo la reazione:
AlCl3 + 3 NaOH -> Al(OH)3 + 3 NaCl
Per questa reazione si pesa una quantità di idrossido di sodio tale da neutralizzare completamente la quantità di acido aggiunto in precedenza e la si discioglie in acqua distillata. La soluzione di soda ottenuta si lascia raffreddare e si aggiunge lentamente alla soluzione acida di cloruro di alluminio facendo attenzione ad eventuali schizzi in caso la temperatura della soluzione salga troppo. A questo punto dovreste vedere che in soluzione si è formata una massa bianca (l’idrossido di alluminio) quindi, dopo aver mescolato un po’ si filtra il solido bianco e lo si pone in un altro barattolo (la soluzione rimanente non è più di alcuna utilità), si aggiunge dell’acqua distillata e lo si lava mescolando e frammentando la massa bianca. Ovviamente, più volte si ripete questo lavaggio meglio è in termini di purezza – tre lavaggi in genere sono più che sufficienti.
Dopo aver eseguito i lavaggi si filtra l’idrossido di alluminio e lo si calcina per disidratarlo e trasformarlo nell’ossido di alluminio (Al2O3) che è il costituente principale del rubino. L’ossido ottenuto lo si pone in un mortaio e lo si pesta fino a polverizzarlo (non serve che sia una polvere impalpabile ma comunque non si possono usare grani grossi). A questo punto si pesa la massa di ossido di alluminio polverizzata e si aggiunge l’ossido cromico (1%, meglio scarso che abbondante, rispetto alla massa di ossido di alluminio) il quale, in caso non sia in polvere va anche lui pestato. Si mischiano intimamente le due polveri in quanto la miscela dev’essere il più uniforme possibile.
Siamo arrivati ora alla parte finale in cui la polvere verrà trasformata nel minerale. Per fare ciò bisogna fondere la polvere e dal momento che l’ossido di alluminio fonde a 2050°C sarà necessaria una fiamma ad idrogeno o ad acetilene oltre ad un supporto fatto di un materiale in grado di resistere a quelle temperature – la grafite andrà benissimo. Per facilitare la fusione conviene trattare piccole quantità di materiale per volta e procedere aggiungendo piccole quantità di polvere ogni volta che la parte precedente è fusa invece che tentare di fondere tutta la povere che avete in un colpo solo. Man mano che la massa fusa torna solida si può osservare che il solido ottenuto ha cambiato colore in quanto cristallizzando è diventato un rubino.
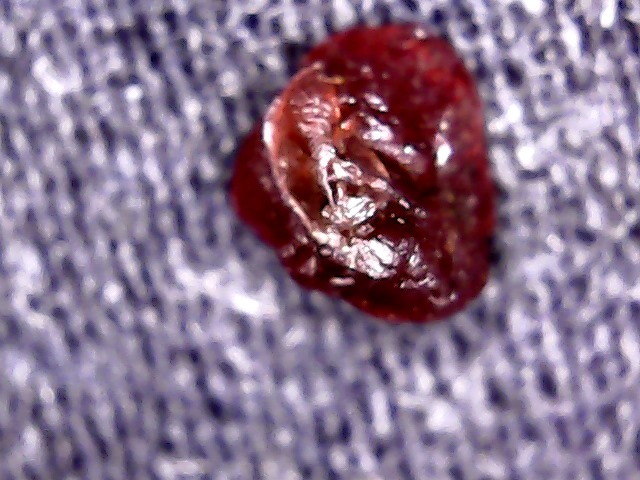
rubino
Note:
Il sito non si assume alcuna responsabilità per danni alla persona o cose.
Chimico industriale:
Michele V.
Immagini:
Wikipedia,
COI.

